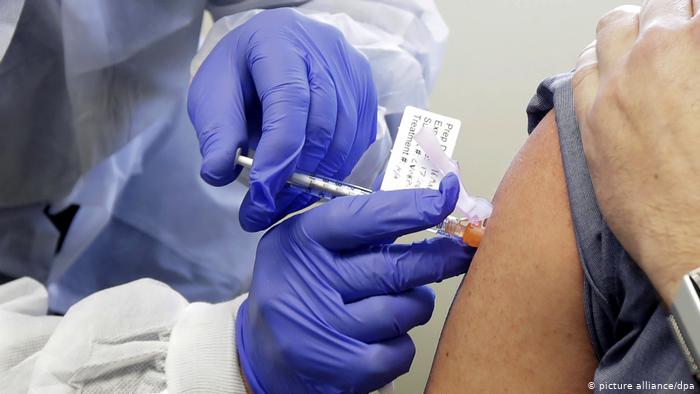
La empresa Moderna presentó solicitudes de emergencia de autorización para su vacuna contra COVID-19 en Estados Unidos y en Europa, luego de que resultados completos confirmaran una alta eficacia de la misma (94,1%).
La compañía farmacéutica Moderna anunció hoy que ha solicitado la autorización para comercializar su vacuna contra el coronavirus tanto a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) como a la Agencia Europea del Medicamento (EMA).
Los reguladores analizarán los datos de prueba de la vacuna de ARNm y decidirán si es lo suficientemente segura y efectiva como para recomendar su implementación.
Dos semanas después de haber anunciado una eficacia de 94,5% sobre la base de resultados preliminares, Moderna reportó que de 196 participantes en su ensayo clínico que se infectaron con COVID-19, 185 pertenecían al grupo placebo y 11 al grupo vacunado, con una eficacia calculada de 94,1%. Ninguna forma grave de la enfermedad se registró en el grupo vacunado.
DW.